近日,上海交通大学农业与生物学院张欢团队与自动化与感知学院张宏陆团队、四川大学华西医院罗耀团队合作,在高水平学术期刊Journal of the American Chemical Society上发表了题为“Dynamic Modulation of Multicellular Interactions via ATP-Dissipative DNA Assembly” (J. Am. Chem. Soc. 2025, 147, 28277)的最新研究成果 。该研究工作利用DNA的可编程性和分子识别能力,构建了一种由ATP驱动的耗散自组装系统,实现了对活细胞间相互作用的动态、可逆和时空精准的调控,并将这一策略有效地应用于肿瘤免疫治疗中。该系统模拟了生物系统中能量依赖的瞬时相互作用,为开发新型智能生物材料和免疫疗法提供了全新思路。

生命体是一个开放的、远离热力学平衡态的复杂系统。其中,细胞间的动态相互作用构成了组织发育、免疫应答以及神经网络形成等关键生命过程的基础。这些过程在时空上受到精确调控,并持续消耗三磷酸腺苷(ATP)等“燃料”以维持系统的动态稳态与非平衡特征。然而,现有用于人工调控细胞相互作用的手段如基因工程或化学修饰,往往只能产生静态或不可逆的细胞连接,难以模拟生物体系中依赖能量耗散的、可逆且自适应的动态行为。
本研究的创新之处在于构建了一个由ATP驱动的酶促反应网络,实现了对细胞间动态组装与解散过程的精准调控。研究团队设计了多种DNA功能单元(包括双链DNA、四面体框架核酸以及支链框架核酸),并通过胆固醇修饰将其锚定于细胞膜表面,从而构建出可控的“能量驱动”细胞组装平台(图1)。
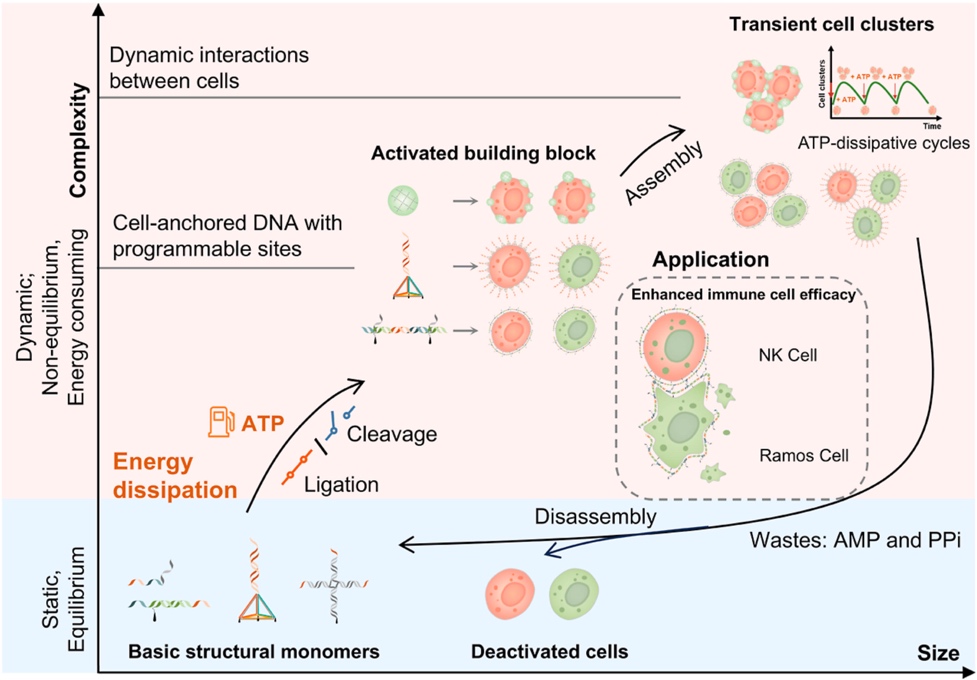
图1. ATP耗散的核酸多层次动态组装与活细胞时空调控
该系统的核心机制在于T4 DNA连接酶与BamHI限制性内切酶所形成的拮抗式酶促反应网络。组装阶段:在外界ATP燃料供给下,T4 DNA连接酶被激活,催化细胞膜表面DNA“零件”之间的磷酸二酯键形成,从而像“分子拉链”一样将细胞紧密连接,形成可控的细胞簇结构。解散阶段:随着反应的持续进行,ATP被逐渐消耗,当其浓度下降至阈值以下时,连接酶失活,而BamHI内切酶开始切断已形成的DNA连接链,导致细胞簇的解体,实现细胞从聚集到分散的可逆转变。
该ATP驱动系统能够在Ramos细胞和PC-12细胞中实现可编程的动态组装与解散。通过调节初始ATP浓度,可以精确控制细胞聚集的时间尺度与程度,展现出良好的能量依赖性和时空可控性。更进一步地,研究团队利用支链框架核酸引入了液-液相分离(LLPS)机制,在细胞膜表面形成类似“细胞外基质”的DNA凝聚体,从而实现更稳定且多层次的细胞组装结构。通过周期性地补充ATP燃料,系统可实现至少三轮高效、可逆的细胞聚集-分离循环,且细胞在整个过程中保持较高的活性和存活率。
该系统不仅能够响应外源添加的ATP,还能对细胞自身分泌的内源性ATP信号作出响应,尤其是该系统展现出了在肿瘤免疫治疗中的重要潜力(图2)。自然杀伤细胞(NK细胞)是免疫系统中能够直接识别并杀伤肿瘤细胞的重要效应细胞,但其抗肿瘤效率常受限于与肿瘤细胞之间不足的接触与识别效率。为此,研究团队将ATP驱动的DNA耗散系统分别修饰于NK细胞和Ramos肿瘤细胞表面,构建出一种可能量调控的细胞桥联系统。在外源ATP的驱动下,T4 DNA连接酶介导的动态“组装”过程可迅速促进NK细胞与肿瘤细胞之间的紧密结合,从而显著增强细胞间的免疫突触形成与杀伤效应。体外细胞实验表明,加入ATP后,NK细胞对肿瘤细胞的杀伤效率在30分钟内迅速提升,肿瘤细胞死亡率高达约80%,显著高于无ATP对照组。更为重要的是,在活体(in vivo)小鼠模型中,该ATP耗散系统赋能的NK细胞表现出显著的肿瘤抑制作用,能有效延缓肿瘤生长进程,同时未观察到明显的毒副作用或组织损伤。这表明,该系统不仅实现了对细胞间动态相互作用的可逆能量调控,也为构建新一代能量驱动型免疫细胞治疗平台提供了全新的思路。

图2. ATP耗散系统调控活体肿瘤细胞免疫杀伤
研究意义
这项研究通过将框架核酸技术与非平衡自组装机制相结合,构建了一个可在能量调控下实现细胞间可逆组装与解离的动态体系。该体系能够在时空尺度上精准调控细胞间的相互作用,模拟了生命体系中能量耗散驱动的动态行为。更重要的是,该平台在肿瘤免疫治疗中展现出显著优势,显著增强了NK细胞与肿瘤细胞的结合与杀伤效率。该研究为构建能量驱动型人工生命系统与细胞免疫治疗平台提供了新的策略方法。
文章信息
上海交通大学自动化与感知学院张宏陆、农业与生物学院张欢为论文的共同通讯作者,四川大学华西医院罗耀、已毕业生研究生徐翼与路晓云为共同第一作者。研究得到了上海交大樊春海院士的指导与支持,并获得国家重点研发计划、国家自然科学基金等项目资助。
文章链接 https://doi.org/10.1021/jacs.5c08925
张欢课题组受邀在国家自然科学基金委员会主管、主办的综合性英文学术期刊Fundamental Research“未来生物材料”专题发表关于可编程生物材料的综述文章(Fundamental Research 2025, 5(4): 1384-1400),系统综述了以框架核酸为代表的可编程生物材料的在仿生矿化模板、骨组织递送系统等方面的研究进展,并详细探讨了其发展挑战和未来前景。骨缺损治疗仍面临多种局限,可编程DNA生物材料凭借独特的生物相容性和结构可控性,为骨再生材料开辟了新路径。


文章链接 https://doi.org/10.1016/j.fmre.2024.12.015
研究团队介绍
上海交通大学农业与生物学院张欢团队,主要研究方向为以核酸技术等纳米尺度构筑操纵手段为核心,实现对生命过程的模拟、调控及监测,拓展其在生命健康、农业与环境与可持续发展等领域的应用。相关研究成果以第一/通讯作者发表于《Nature Nanotechnology》《Nature Communications》《PNAS》《Nature Protocols》《JACS》等高水平学术期刊,申请发明专利与软件著作十余项,并积极开展颠覆性技术的概念验证研究。欢迎感兴趣的同仁加入团队共谋发展!联系邮箱: zhang_huan@sjtu.edu.cn
